尊敬的用户:根据《医疗器械监督管理条例》企业经营医疗器械提供相关经营资质,谢谢配合!
注册证号:国械注进20173067126 有效期截止:2027/11/28

找维修

找配置

找授权

找证件

找寰熙

延续注册产品技术要求未发生变化,沿用原核发的产品技术要求。原注册证编号:国械注进20173307126
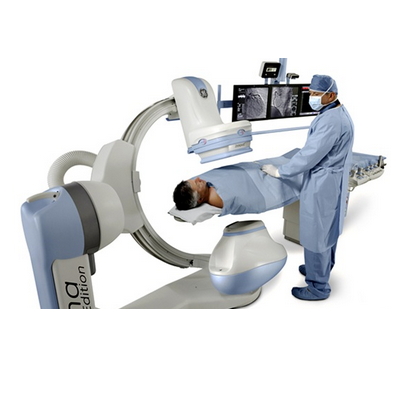
2017-03-31 变更对比表详见附件。 2019-04-12 1、型号规格由“Innova IGS 520”变更为“Innova IGS 5”;2、结构及组成由“由基本硬件、可选硬件、软件选件组成,其中基本硬件包括机架(含定位器:包括L形臂、C形臂)、检查床Omega V、Omega IV或Innova-IQ、床旁用户接口(智能盒或智能手柄、床旁状态控制器)、高压发生器、X射线管组件(含X射线管、X射线管套)、限束器、C1控制柜和C2控制柜、数字探测器、室内监视器和控制监视器(黑白监视器、DL彩色监视器、彩色监视器)、冷却器(探测器冷却器、球管冷却器)、DL键盘、VCIM、患者附件、蜂鸣箱、红外发射器及接收器、20kVA Fluoro UPS和电源分配柜组成。可选硬件、软件选件(发布版本:IGS 5_2)详见产品技术要求。”变更为“产品由机架、高压发生器、X射线管组件、限束器、数字平板探测器、C-FRT机柜、检查床、PDU、UPS、监视器、冷却器、操作员控制台、附件及选件组成。”;3、产品技术要求发生变化,新的产品技术要求替换原有内容。新的产品技术要求详见附件。 2019-11-12 1.原注册证中结构及组成由“产品由机架、高压发生器、X射线管组件、限束器、数字平板探测器、C-FRT机柜、检查床、PDU、UPS、监视器、冷却器、操作员控制台、附件及选件组成。”变更为“产品由机架、高压发生器、X射线管组件、限束器、数字平板探测器 (20.5 cm,31 cm,41 cm)、C-FRT机柜、检查床、PDU、UPS、监视器、冷却器、操作员控制台、附件及选件组成。” 2.原注册证中注册人名称由“GE MEDICAL SYSTEMS SCS”变更为“GE MEDICAL SYSTEMS SCS 通用电气医疗系统两合公司”。